Десятилетиями терапия на основе антител трансформировала современную медицину, однако всегда существовало фундаментальное биологическое препятствие: антитела не способны проникать внутрь клеток. Традиционные антитела слишком велики, чтобы преодолевать клеточную мембрану, что ограничивает их способность воздействовать на заболевания, возникающие внутри клетки. Тем не менее, новые исследования предполагают, что этот барьер вскоре может быть преодолен, что открывает перспективное новое направление для лечения муковисцидоза и потенциально других генетических нарушений.
Инженерным путем создав «нанотела» — крошечные, компактные фрагменты антител, — ученые разработали терапию, способную проникать сквозь клеточные стенки и стабилизировать дефектные белки изнутри. Это прорывное решение не только улучшает функцию белка, ответственного за муковисцидоз, но и значительно повышает эффективность существующих методов лечения, приближая состояние клеток пациентов к нормальному уровню здоровья.
Проблема традиционных антител
Чтобы понять значимость этого достижения, необходимо рассмотреть ограничения современных препаратов на основе антител. Хотя они высокоэффективны при нацеливании на поверхностные рецепторы или циркулирующие патогены, антитела полного размера физически не способны проходить через липидный бислой клеточных мембран. Следовательно, они могут взаимодействовать только с мишенями, находящимися снаружи клеток.
Муковисцидоз, однако, является внутриклеточной проблемой. Заболевание вызвано мутацией в гене CFTR, в результате которой производится неправильно свернутый белок, не способный достичь поверхности клетки. Текущие методы лечения используют низкомолекулярные препараты, помогающие этому белку правильно свернуться или лучше функционировать, но такие терапии редко восстанавливают его полную естественную функциональность. Болезненный процесс начинается внутри клетки, однако традиционные технологии антител не могли до него добраться.
Появление нанотел
Решение кроется в нанотелах. Впервые выделенные из верблюдовых (таких как верблюды и ламы), это однодоменные фрагменты антител, которые значительно меньше и стабильнее обычных антител. Их компактный размер позволяет эффективнее проникать в ткани, но одного размера было недостаточно для преодоления клеточной мембраны.
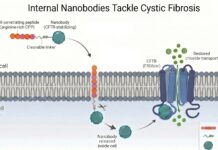
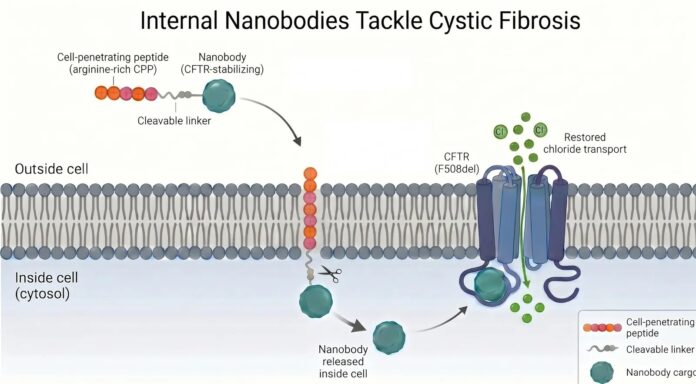
Исследователи решили проблему доставки, соединив нанотело с клеточно-проницаемым пептидом. Этот пептид состоит из десяти положительно заряженных аминокислот аргинина. Поскольку клеточные мембраны имеют отрицательный заряд, пептид взаимодействует с поверхностью клетки, облегчая ее поглощение внутрь. Попасть внутрь клетки, нанотело высвобождается, чтобы найти свою специфическую мишень.
Ключевой момент: Без этой молекулярной «ключи» (пептида) нанотело оставалось бы вне клетки, бесполезным для внутриклеточных мишеней. Это слияние создает гибридную молекулу, способную преодолевать клеточный барьер.
Стабилизация сломанного белка
У пациентов с муковисцидозом мутантный белок CFTR нестабилен и имеет неправильную форму. Он застревает внутри клетки и разрушается до того, как успевает достичь поверхности для регуляции транспорта соли и воды. Это приводит к образованию характерной густой, липкой слизи, забивающей легкие.
Новое нанотело связывается непосредственно с нестабильной областью белка CFTR. Прикрепляясь к нему, нанотело действует как структурный каркас, стабилизируя неправильно свернутый белок. Такая стабилизация позволяет белку правильно созреть, избежать деградации и добраться до клеточной мембраны. По прибытии он возобновляет свою роль как функциональный хлоридный канал, обеспечивающий правильный баланс жидкостей.
Синергия с существующими терапиями
Возможно, самым убедительным выводом этого исследования является то, как этот новый подход дополняет существующие методы лечения. Текущие одобренные препараты для лечения муковисцидоза стабилизируют другие области белка CFTR. Нанотело нацелено на отдельный домен, затронутый мутацией.
При совместном использовании эти методы усиливают друг друга:
- Усиленная активность: В клеточных моделях сочетание нанотела со стандартными комбинациями препаратов привело к существенному росту активности CFTR по сравнению с любым из методов по отдельности.
- Функция, близкая к нормальной: В клетках дыхательных путей, полученных от пациентов, такая комбинированная терапия восстановила функцию белка почти до 90% нормального уровня. Это значительный шаг вперед, предполагающий, что пациенты могут испытать радикальное улучшение здоровья легких и снижение накопления слизи.
За пределами муковисцидоза
Хотя непосредственный фокус направлен на муковисцидоз, последствия этой технологии распространяются гораздо дальше этого одного заболевания. Возможность доставлять функциональные белковые препараты внутрь клеток открывает путь к лечению широкого спектра состояний, при которых внутриклеточные белки работают с ошибками — от редких генетических нарушений до распространенных болезней со сложными внутренними механизмами.
Предыдущие попытки доставки белков в клетки часто опирались на генную терапию, которая включает в себя введение генетического материала в клетки, чтобы заставить их производить терапевтический белок. Этот подход несет в себе собственные риски и сложности. Метод с использованием нанотел, напротив, доставляет белок напрямую, не изменяя ДНК пациента, предлагая потенциально более безопасный и прямой путь к лечению.
Вызовы и будущие направления
Несмотря на перспективы, преграды остаются. Основной вызов — это доставка в сложных средах, таких как легкие человека, где густая слизь может блокировать доступ к целевым клеткам. Для уточнения способов введения этих нанотел, чтобы гарантировать их попадание в нужные клетки в достаточном количестве, необходимы дальнейшие исследования.
Однако доказательство концепции теперь очевидно: белковые препараты можно спроектировать так, чтобы они преодолевали клеточные барьеры и исправляли механизмы заболевания у их истока. Этот прорыв расширяет горизонты того, чего могут достичь терапии на основе антител, переводя медицину с поверхности клетки во ее внутренность.
Подводя итог, можно сказать, что это нововведение представляет собой сдвиг парадигмы в разработке лекарств. Обеспечивая проникновение нанотел в клетки и стабилизацию дефектных белков, ученые открыли новый уровень точности в лечении генетических заболеваний, давая надежду на более эффективные и комплексные терапии в ближайшем будущем.